
La interferencia
La difracción
La energía era de naturaleza continua
y la energía electromagnética era proporcional a la amplitud de una onda.
Experimentos cruciales:
Experimentos cruciales:
- El espectro discontinuo de emisión del Hidrógeno.
- El efecto fotoeléctrico.
FÍSICA MODERNA
La energía era de caracter discontinuo

se presenta en forma de pequeños "paquetes de enegía", que se denominan cuantos, cuantas o fotones.
La energía electromagnetica es proporcional a su frecuencia
Ecuación de Planck:
energía de un foton = hv donde h= Constante de Planck = 6,62 10 -27 erg. seg
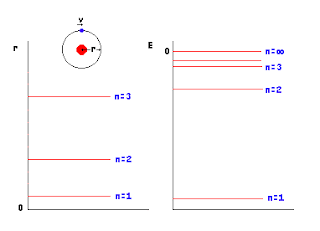
EL ATOMO DE HIDROGENO DE BOHR
1) Orbitas circulares
2) Momento angular = m e v r = n h / 2 p n = 1,2,3...........a
2) Momento angular = m e v r = n h / 2 p n = 1,2,3...........a
Ciertos valores de r Ciertos valores de E
u órbitas permitidas o niveles de energía permitidos
u órbitas permitidas o niveles de energía permitidos
Energía asociada a los cambios de órbita
E fotón absorbido= E(final) - E(inicial) E fotón emitido= E(inicial) - E(final)
LA MECANICA CUANTICA ONDULATORIA
DE BROGLIE " Todo cuerpo en movimiento tiene una onda asociada"
λ = h / m x v = h / p
NÚMEROS CUÁNTICOS
Los números cuánticos son valores numéricos que nos indican las características de los electrones de los átomos, esto esta basado desde luego en la teoría atómica de Neils Bohr que es el modelo atómico mas aceptado y utilizado en los últimos tiempos.Los números atómicos más importantes son cuatro:
Número Cuántico Principal.
Número Cuántico Secundario.
Número Cuántico Magnético.
Número Cuántico de Spin.
Número Cuántico Principal (n)El número cuántico principal nos indica en que nivel se encuentra el electrón, este valor toma valores enteros del 1 al 7.
Número Cuántico Secundario (d)Este número cuántico nos indica en que subnivel se encuentra el electrón, este número cuántico toma valores desde 0 hasta (n - 1), según el modelo atómico de Bohr - Sommerfield existen además de los niveles u orbitas circulares, ciertas órbitas elípticas denominados subniveles. Según el número atómico tenemos los numeros:
l = 0 s sharp
l = 1 p principal
l = 2 d diffuse
l = 3 f fundamental
l = 4 g
l = 5 h
l = 6 i
l = 0 s sharp
l = 1 p principal
l = 2 d diffuse
l = 3 f fundamental
l = 4 g
l = 5 h
l = 6 i
Número Cuántico Magnético (m) El número cuántico magnético nos indica las orientaciones de los orbitales magnéticos en el espacio, los orbitales magnéticos son las regiones de la nube electrónica donde se encuentran los electrones, el número magnético depende de l y toma valores desde -l hasta l.
Número Cuántico de Spin (s) El número cuántico de spin nos indica el sentido de rotación en el propio eje de los electrones en un orbital, este número toma los valores de -1/2 y de 1/2. De esta manera entonces se puede determinar el lugar donde se encuentra un electrón determinado, y los niveles de energía del mismo, esto es importante en el estudio de las radiaciones, la energía de ionización, así como de la energía liberada por un átomo en una reacción.
Principio de Exclusión de Pauli
El mismo dice "En un mismo átomo no puede existir dos electrones que tengan los mismos números cuánticos" de esta manera podemos entonces afirmar que en un mismo orbital no puede haber más de dos electrones y que los mismos deben tener distinto número de spin.
Regla de Hund
Cuando se llena orbitales con un mismo nivel de energía o lo que es lo mismo que se encuentran en un mismo subnivel se debe empezar llenando la mitad del subnivel con electrones de spin +1/2 para luego proceder a llenar los subniveles con electrones de spin contrario (-1/2).
Principio de Estabilidad o menor Energía







No hay comentarios:
Publicar un comentario